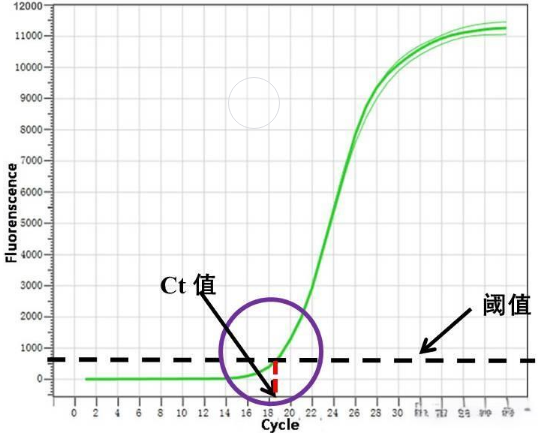
阈值循环数 Threshold cycle (Ct) 也写作Cq值,荧光信号大于荧光阈值时PCR循环数。仪器软件通常将第3-15个循环的荧光值设为基线(baseline),是由于测量的偶然误差引起的。阈值(threshold)一般是基线的标准偏差的10倍。在实际操作中也可以手动调节。高于阈值的荧光信号被认为是真实的信号,用于定义Ct值。Ct会受到阈值的影响,每次试验由于样品和仪器的不同会导致基线不同,进而影响阈值和Ct值。
模板的Ct值与该模板的起始拷贝数的对数存在一定线性关系,起始模板量浓度越高,Ct值越小;起始模板量浓度越低,Ct值越大。PCR循环在到达Ct值所在的循环数时,刚刚进入真正的指数扩增期(对数期),此时微小误差尚未放大,Ct值的重现性较好,即相同含量的初始模板,得到的Ct值是相对稳定的。
Ct值不是恒定不变的,可以受到不同样品、不同仪器的影响,即使相同的样品在相同的仪器上重复2遍,Ct值也会存在差异。
为什么要有Ct值?
➤ 模板量与Ct值的关系:
在PCR指数扩增过程当中,产物量与循环数之间的关系是:扩增产物量=起始模板量×(1+En)循环个数。
➤ Ct值的设定:
qPCR扩增产物量是以荧光信号的形式直接呈现,也就是扩增曲线。在扩增过程当中,设定一个荧光信号值,当扩增产物量达到“一定产物量”时(即达到此荧光阈值时),此时循环数定义为Ct值,需要注意的是,Ct值需要处于指数扩增时期。因此Ct值与起始模板量的关系:模板的Ct值与该模板的起始拷贝数的对数存在线性关系。起始模板量浓度越高,Ct值越小;起始模板量浓度越低,Ct值越大。
➤ Ct值的重现性
Ct值是荧光定量PCR最重要的结果呈现形式,用于基因表达量差异或基因拷贝数的结果计算。一般情况下,复孔Ct值的差值最好不超过0.05,不然表明误差结果太大,结果不可信。在PCR早期,扩增处于理想情况下,循环数较少,产物积累少,产生荧光的水平不能与荧光本底背景明显的区别;之后荧光的产生增加进入指数期,此时微小误差尚未放大,Ct值的重现性极好,即同一模板不同时间扩增或同一时间不同管内扩增,得到的Ct值是恒定的。
1、与Ct值有关的参数
标准曲线Standard curve:模板的Ct值与该模板的起始拷贝数的对数存在线性关系。利用已知起始拷贝数的标准品可作出标准曲线,其中横坐标代表起始拷贝数的对数,纵坐标代Ct值。
相关系数Correlation coefficient (R^2) :反映了标准曲线的线性,通常要求>0.99。
扩增效率Efficiency (E):通常要求在90%~110%。效率低于100%,是由于PCR反应中存在抑制因素;而高于100%可能一些污染、非特异性扩增或者是引物二聚体造成。
斜率Slope :当扩增效率为100%时斜率为-3.32,当90%-110%时的斜率为-3.58 ~ -3.10。
2、Ct值与模板拷贝数的关系
理想情况下,qPCR的模板经过一定的循环数进行指数扩增,扩增循环数和产物量之间的关系是:扩增产物量Cn=起始模板量C1×(1+扩增效率E)^循环数n。但是由于E通常无法达到100%,并且在扩增的后期,扩增效率会逐渐降低,只有在理想的情况下才满足Cn=C1×2^n,即Ct值差1,初始浓度差2倍。
由于Ct值与起始模板的对数存在线性关系,可利用标准曲线对未知样品进行定量测定。这是目前的qPCR定量的方法,即用已知浓度的标准品与未知浓度样品同时扩增,将未知浓度样品的Ct值代入该标准曲线获得未知样品浓度。分析定量时,一般取Ct:15-35。太大或者太小都会导致定量结果的不准确。标准曲线需满足:E:90%~110%,R^2≥0.99,斜率-3.58 ~ -3.10。同时定量标准品的量值需要准确可靠。用qPCR进行定量,理论上可行,实际上很难获得准确的定量结果。
3、Ct值异常的原因与解决方案